6月25日,澳门威斯人0168徐华娥教授团队在国际知名学术期刊《先进功能材料》(Advanced Functional Materials)(中科院1区,IF=18.5)在线发表了最新研究成果《基于TIM3沉默纳米佐剂和去唾液酸化肿瘤细胞膜抗原的双重增强型新型纳米疫苗用于癌症的个性化疫苗免疫治疗》(A Dual Enhancing Strategy of Novel Nanovaccine Based on TIM3 Silencing Nanoadjuvants and Desialylated Cancer Cell Membrane Antigens for Personalized Vaccination Immunotherapy of Cancer)。

肿瘤疫苗是一种前景广阔的癌症治疗疗法。然而,目前肿瘤疫苗引发抗肿瘤免疫反应的效率有限,尚未取得令人满意的结果。最新研究发现,导致肿瘤疫苗疗效不佳的重要原因包括以下因素:如树突状细胞(Dendritic cells, DCs)的功能受到关键免疫检查点T细胞免疫球蛋白粘蛋白分子3(T cell immunoglobulin and mucin-containing molecule 3, TIM3)的抑制、单一肿瘤抗原的免疫原性较弱以及疫苗进入淋巴结的效率受纳米尺寸限制等。因此,本研究针对上述问题设计了一种新型肿瘤纳米疫苗。首先,针对DCs的关键免疫检查点TIM3设计了一种新型纳米佐剂(LNP/siRNA),其可在沉默免疫检查点TIM3的同时激活Toll样受体,从而增强DCs的免疫活性。其次,针对单一肿瘤抗原免疫原性弱的问题,我们采用去唾液酸化肿瘤细胞膜为DCs提供多样性的个性化肿瘤抗原,以增强DCs的抗原呈递功能。最后,我们将LNP/siRNA佐剂与去唾液酸化肿瘤细胞膜抗原相结合制成一体化新型肿瘤纳米疫苗(dClip-LNP/siRNA),实现双重增强肿瘤疫苗疗效的目的。
本研究结果显示,dClip-LNP/siRNA纳米疫苗能有效进入淋巴结,显著抑制DCs中TIM3的表达、促进DCs的抗原呈递,进而促进T细胞的活化,并诱导产生强大而持久的抗肿瘤免疫反应。此外,dClip-LNP/siRNA纳米疫苗还可与过继OT-I细胞疗法结合,联合增强癌症免疫治疗疗效。该研究提供了一个有效的个性化肿瘤纳米疫苗平台,为癌症免疫治疗提供了新的思路。
该论文通讯作者为澳门威斯人0168徐华娥教授;第一作者为徐华娥教授课题组博士后李凯明;共同第一作者为南京医科大学第一附属医院李晓林副教授,以及徐华娥教授课题组2022级硕士吴洁和2020级博士吴海斯。
该研究得到了国家自然科学基金、江苏省重点研发计划(社会发展)面上项目、南京医科大学高层次人才启动基金等项目的资助。
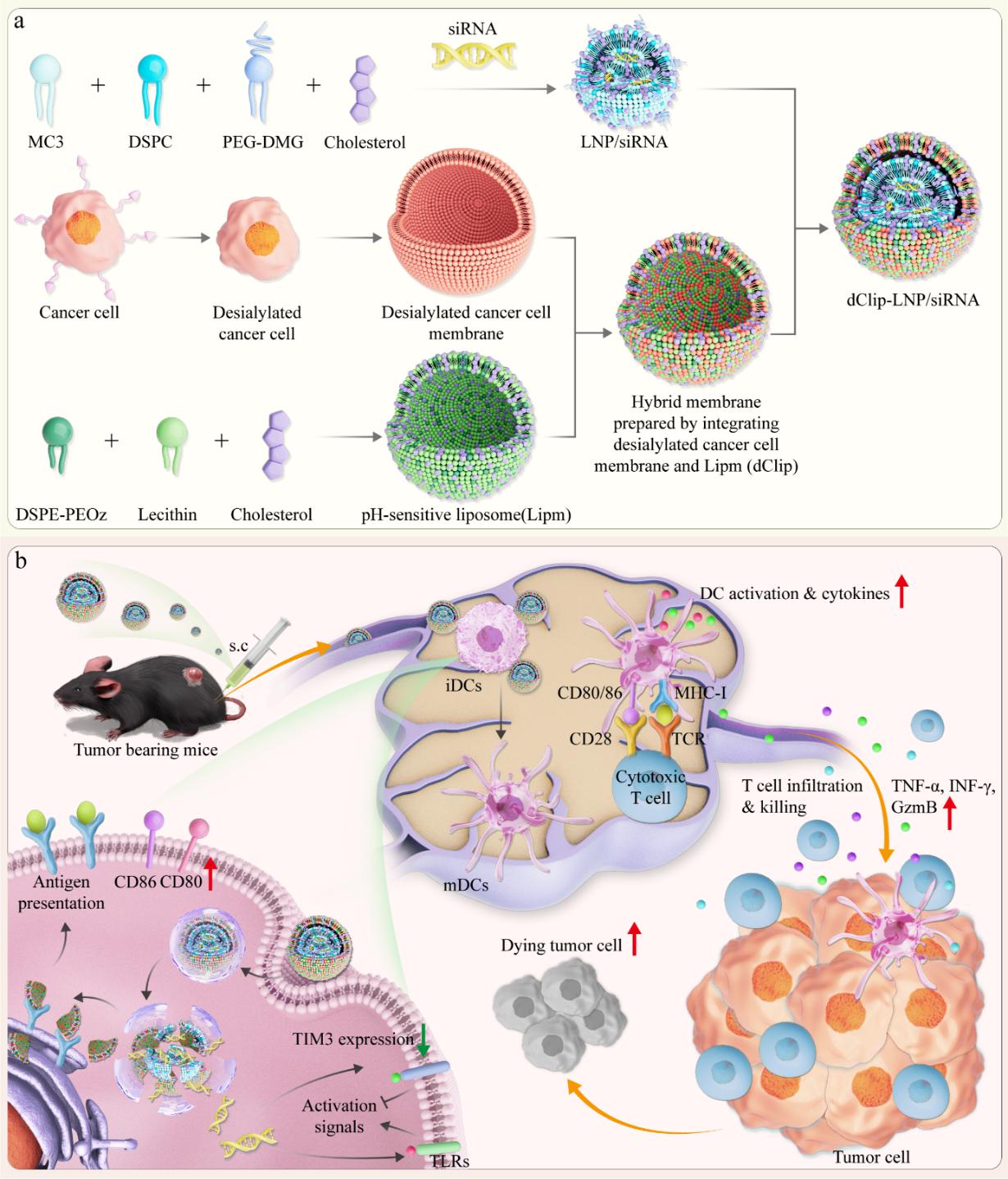
Model:Schematic illustration of the preparation of dClip-LNP/siRNA and its mechanism for inducing antitumor immune responses.
模型图:dClip-LNP/siRNA的制备及其诱导抗肿瘤免疫反应机制的示意图。
原文链接:
https://onlinelibrary.wiley.com/doi/abs/10.1002/adfm.202404956
(撰稿/徐华娥课题组;审核/陈宏山 刘明捷)


