近日,澳门威斯人0168在疾病组织微环境巨噬细胞与T细胞互作参与稳态调控取得新进展。生物医学工程与信息学院汪强虎教授,我院陈宏山教授,江苏省人民医院 (南京医科大学第一附属医院) 张军霞教授合作在Cancer Research (中科院一区,IF, 13.3) 发表题为“Phagocytosis of glioma cells enhances the immunosuppressive phenotype of bone marrow-derived macrophages” 研究论文,第一作者为我院重点实验室陈宏山教授课题组博士生吴敏;同时江苏省肿瘤医院 (南京医科大学附属肿瘤医院) 冯继峰教授,我院陈宏山教授,生物医学工程与信息学院汪强虎教授合作在Caner Letters (中科院一区,IF, 9.7) 发表题为“Single-cell RNA sequencing unveils the communications between malignant T and myeloid cells contributing to tumor growth and immunosuppression in cutaneous T-cell lymphoma” 研究论文,第一作者为江苏省肿瘤医院冯继峰教授课题组博士生杜雨欣。
细胞外多种免疫细胞及基质构成复杂的细胞分子空间网络,提供特定的组织微环境信号,这种组织微环境稳态调控与疾病的发生发展密切相关,对于肿瘤,心血管疾病及衰老相关疾病等多种病理状态均有重大的影响。肿瘤相关巨噬细胞(Tumor-associated macrophages, TAMs) 在免疫抑制中起着重要作用。然而,TAMs如何转化为免疫抑制表型并影响肿瘤微环境(TME) 尚不完全清楚。通过胶质母细胞瘤(GBM) 组织单细胞RNA测序和全外显子组测序数据,鉴定出双表达巨噬细胞和肿瘤特征TAMs子集,又称为双阳性TAMs,其倾向于骨髓来源的巨噬细胞(BMDMs),具有免疫抑制表型特征。BMDMs体外吞噬胶质瘤细胞产生双阳性TAMs,其免疫抑制表型与GBM TME患者的双阳性TAMs相似。双阳性TAMs转化为M2样巨噬细胞,通过表达免疫检查点蛋白CD276、PD-L1和PD-L2并抑制活化T细胞的增殖来抑制免疫抑制。TME中BMDMs对胶质瘤细胞的吞噬作用导致双阳性TAMs的形成,增强了免疫抑制表型,阐明了驱动TAMs介导的GBM免疫抑制的过程。同时,通过比较来自晚期皮肤T细胞淋巴瘤(CTCL) 患者和健康对照单细胞RNA测序数据,我们发现CTCL中T/NK细胞和髓系细胞明显富集,其中T细胞亚群(CXCR3+, GNLY+, CREM+和MKI67+T细胞),具有高增殖、干性和拷贝数变异(CNV) 水平。此外,CCL13+单核/巨噬细胞和LAMP3+CDC细胞被富集并介导通过与恶性T细胞的相互作用抑制免疫抑制,揭示了T细胞和髓系细胞相互作用介导的免疫抑制TME。
该系列研究为GBM及晚期CTCL患者提供了治疗新靶点和潜在治疗策略。同时该研究成果也为进一步深入目前在研心血管疾病组织微环境稳态调控的分子机制打下坚实的基础。
该研究得到了国家自然科学基金的大力资助,在此表示衷心的感谢!
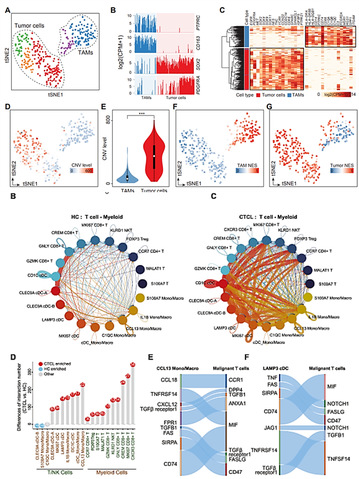
图1 肿瘤微环境中巨噬细胞与T细胞互作分析图
(撰稿人:姜虹;审核:陈宏山)


